0 引言
生物可降解血管支架的发明被誉为冠状动脉介入术的第四次革命[1]。生物可降解血管支架对血管提供短期的支撑后逐渐消失,避免了传统支架永久留在体内而导致的血管舒缩功能受损、晚期支架内再狭窄和晚期靶病变血运重建等问题[2-5]。可降解聚合物血管支架是可降解支架领域的重要研究方向[6-7],但是聚合物材料相比传统支架采用的金属材料其力学性能较弱,在同样的结构下,可降解聚合物血管支架的径向支撑强度要比金属支架的径向支撑强度小得多甚至不能满足临床需求[7-8],因此,如何提高径向支撑强度是解决可降解聚合物血管支架发展的关键问题。
目前,解决该问题除了材料改性[9-11]外主要有两种方法:①增大壁厚[12-14]。虽然增大壁厚可有效提高支架的径向支撑强度,但是壁厚增大会使支架系统外轮廓增大,限制了其对扭曲严重或钙化严重的病变血管的治疗,此外壁厚过大易导致支架内再狭窄和新内膜增生[15]。②改变支架结构。支架结构对径向支撑强度、弯曲刚度、径向回缩率和轴向短缩率等均有较大影响[16-17]。WU等[18]、HSIAO等[19]通过有限元方法研究了类似正弦结构的支撑环对径向支撑强度的影响,结果表明筋宽对其影响较大。然而,这些研究仅改变了支撑环的几何参数,并未研究支架结构形式对径向支撑强度的影响。AZAOUZI等[20]、MORI等[21]研究了不同结构形式的桥筋对弯曲刚度的影响,但是均未考虑桥筋对其他性能的影响。FENG等[22]设计了一种滑扣型可降解聚合物血管支架,并通过实验验证了滑扣型支架的径向支撑强度高于传统的管状镂空结构支架的径向支撑强度,然而滑扣型支架结构复杂,在滑动过程中容易导致局部机械磨损[23]。可见,针对如何提高可降解聚合物血管支架的径向支撑强度尚无理想的解决办法,尤其是通过支架结构设计来解决该问题的研究相对较少。目前检索到的相关报道大多只针对同一支架结构的单一性能进行研究,鲜有对不同支架结构多性能指标的综合研究以及支架结构对性能指标影响规律的研究。
本文针对可降解聚合物血管支架的径向支撑强度不足的问题,研究了支撑单元夹角与其径向支撑强度的关系,在此基础上提出了不等高支撑环结构设计方法,并根据该方法设计了三种支架。采用有限元方法对比分析了该三种支架和雅培公司的生物可降解血管支架(bioresorbable vascular scaffolds, BVS)[1]的径向支撑强度、径向回缩率、轴向短缩率和弯曲刚度,同时研究了支架结构对上述性能的影响规律,以获得具有高径向支撑强度且综合力学性能良好的可降解聚合物血管支架。
1 可降解聚合物血管支架结构设计
血管支架经球囊系统输送至血管病变位置后,通过球囊膨胀使得支架扩张至指定尺寸,然后球囊卸载并撤出,支架最终留在体内对病变血管提供径向支撑以增强血管的畅通性,如图1所示。通常,管状镂空型血管支架由支撑环和桥筋构成,如图2所示。支撑环的主要作用是支撑病变血管,桥筋的主要作用是将相邻两支撑环连接在一起。通常支架直径d<5.0 mm,壁厚c<0.2 mm。要求支撑力F>50.0 N/m,径向回缩率η<15.0%,轴向短缩率μ<10.0%,弯曲刚度k<30.0 N·mm2。
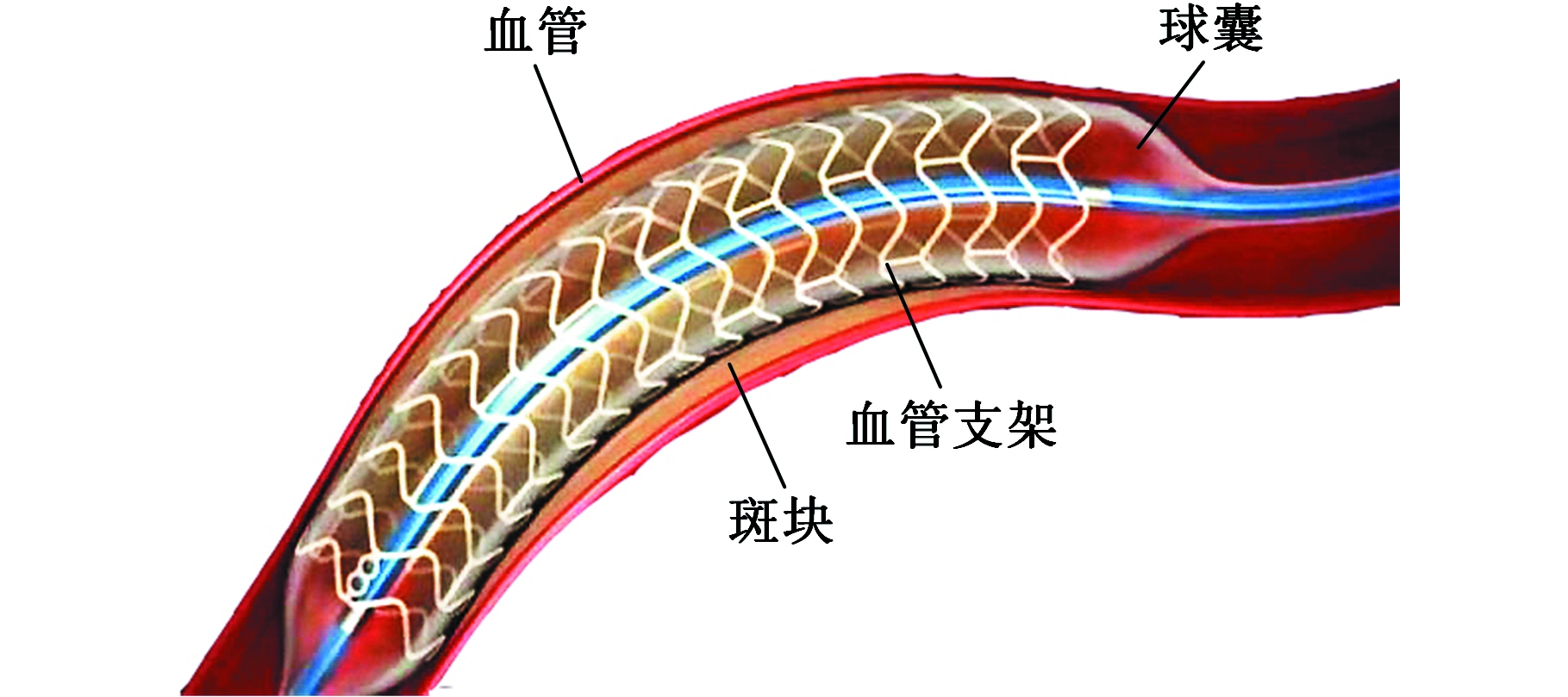
图1 经皮血管支架成形术示意图
Fig.1 Diagram of percutaneous transluminal
stent angioplasty

图2 管状镂空型血管支架
Fig.2 Slotted-tube vascular stent
1.1 支撑环结构设计
血管支架的径向支撑强度主要取决于支撑环,因此支撑环的结构设计至关重要。当支架植入人体后,支架外表面受到血管壁的压力p作用,如图3a所示。由于支撑环由循环交替的若干支撑单元排列构成,为便于分析,取支撑单元的一半为研究对象,如图3b、图3c所示,其中图3b为半支撑单元的正向视图,图3c为半支撑单元的轴向视图。图中,r为支架平均半径,β0近似为支撑单元夹角的一半,α0为半支撑单元周向角度,h为支撑单元高度,w、t分别为筋宽和筋厚。分别在半支撑单元两侧端面定义笛卡儿坐标系oxyz、o′x′y′z′,两坐标系的原点分别位于两端面的形心,x轴和x′轴分别垂直于两端面,y轴和y′轴分别平行于支撑环的轴线,z轴和z′轴沿支撑环的径向方向。在压力p的作用下,半支撑单元的两端部受到力Fx和Fx′、弯矩Mz和Mz′作用,如图3b所示,那么根据对称性和力的平衡方程[24]可以得到:
(1)
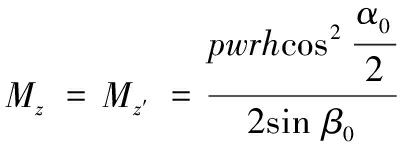
(2)
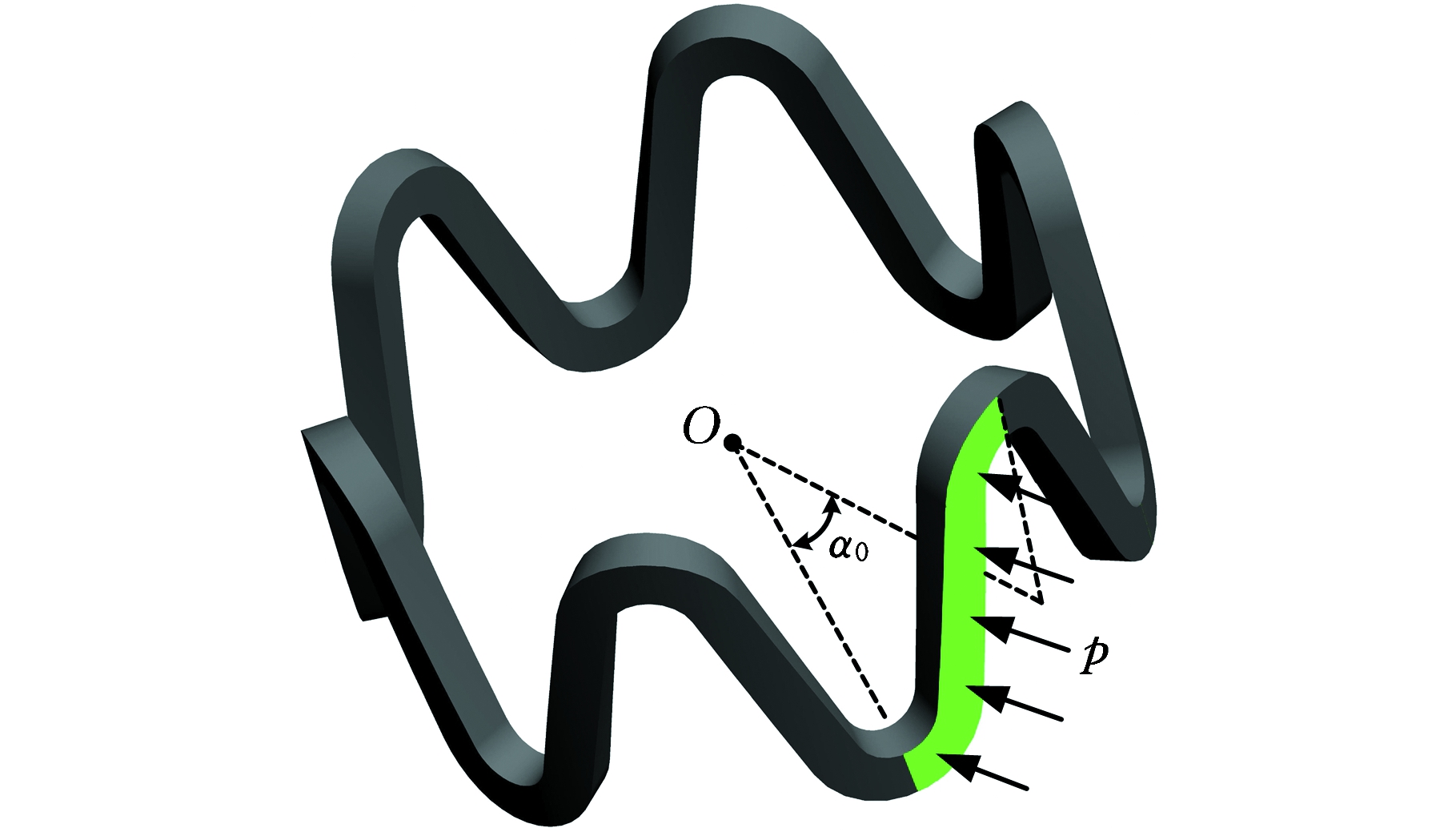
(a)支撑环三维图
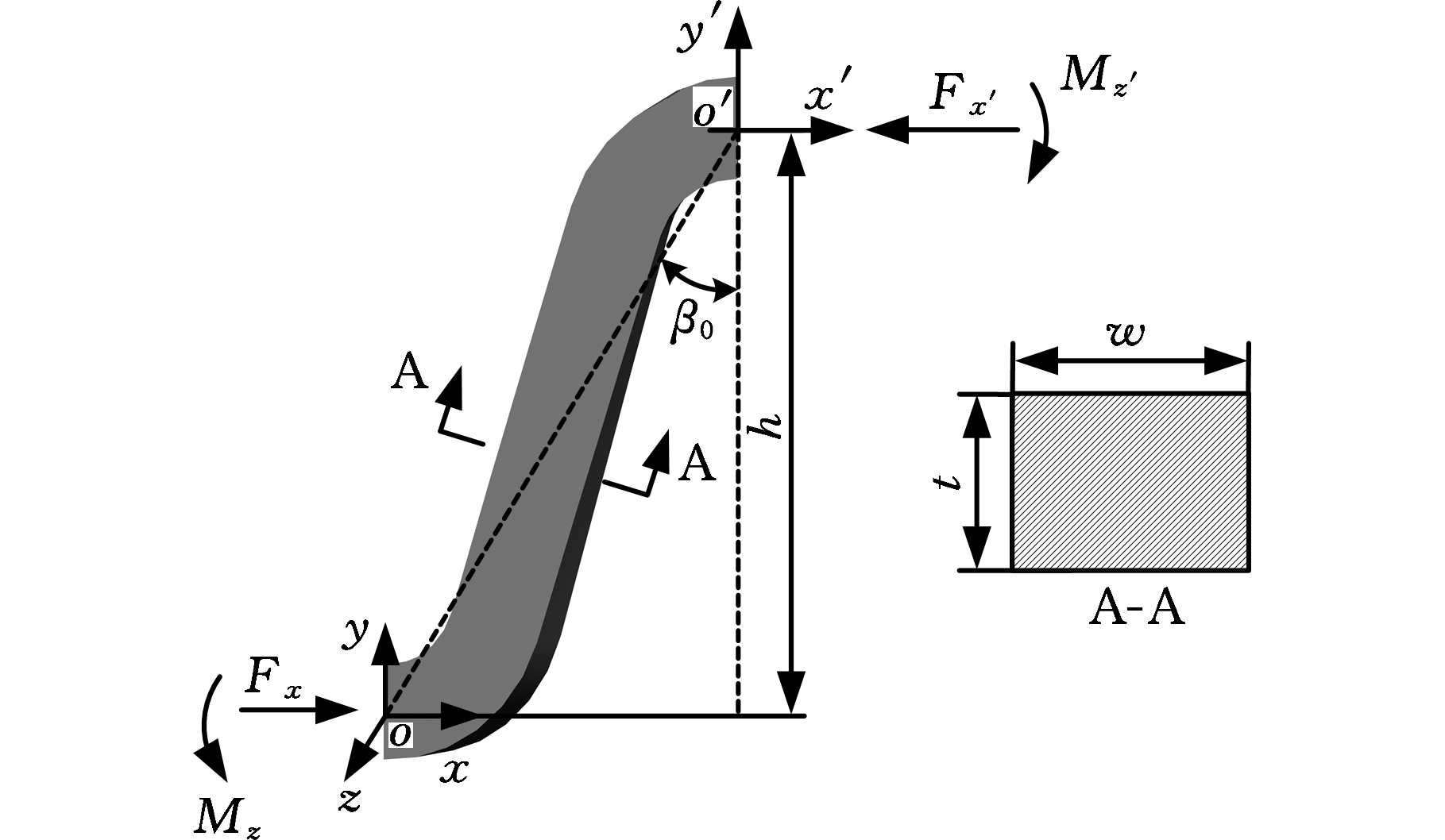
(b)半支撑单元正向视图
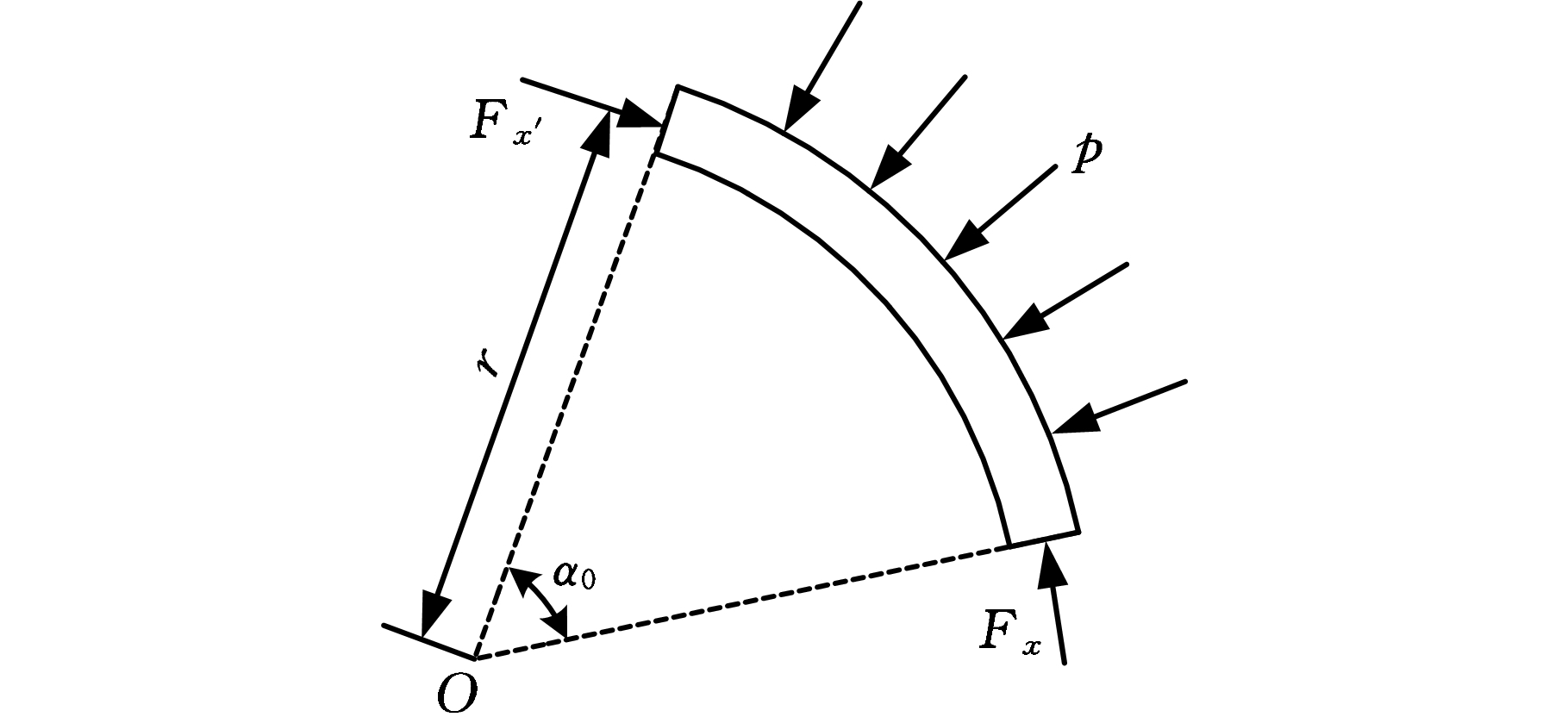
(c)半支撑单元轴向视图
图3 支撑环在外部径向压力作用下示意图
Fig.3 Diagram of supporting ring under external
radial pressure
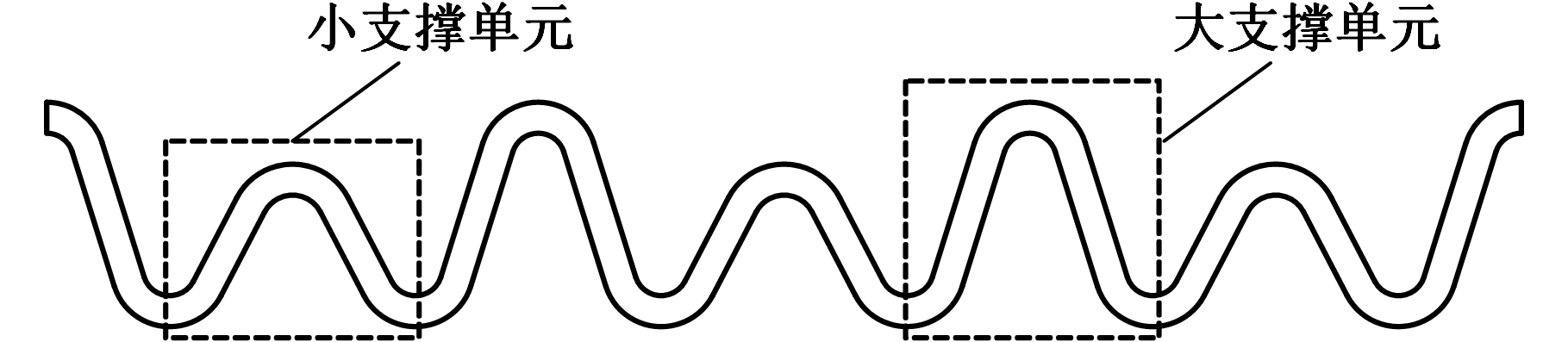
图4 不等高支撑环示意图
Fig.4 Schematic diagram of unequal-height
supporting ring
由式(1)和式(2)可以看出,随着β0的增大,Fx减小,同时由于随着β0增大,支撑单元的高度h减小,因此Mz也减小。而Fx和Mz是引起支架径向变形甚至坍塌的最主要因素,因此,增大支架扩张后的支撑单元夹角,有助于提高支架的径向支撑性能。但是,单纯地将所有支撑单元夹角增大会减小支架的扩张范围,据此,本文提出不等高支撑环结构,即支撑环由高度不同的支撑单元循环交替构成,如图4所示。通过几何分析可知,当周向产生相同位移增量时,扩张前支撑单元夹角越大,扩张后角度增量越大。其几何关系分析如下。
将具有不同高度的支撑单元简化为两个等腰三角形△ABC和△GBC,如图5所示,支撑单元夹角分别对应β1 和β2 ,当底边长度增加Δl时,则两三角形分别转变为△ABE和△GBF,两顶角的增量分别为Δβ1和Δβ2,则
(3)
(4)
经几何推导,得到
cosΔβ1-cosΔβ2=[(BD2+BC2-
2BD·BC·cos∠FBD)·AC2-(BD2+BC2-![]()
(5)
因为AC>GC,则
cosΔβ1-cosΔβ2>![]()
(6)
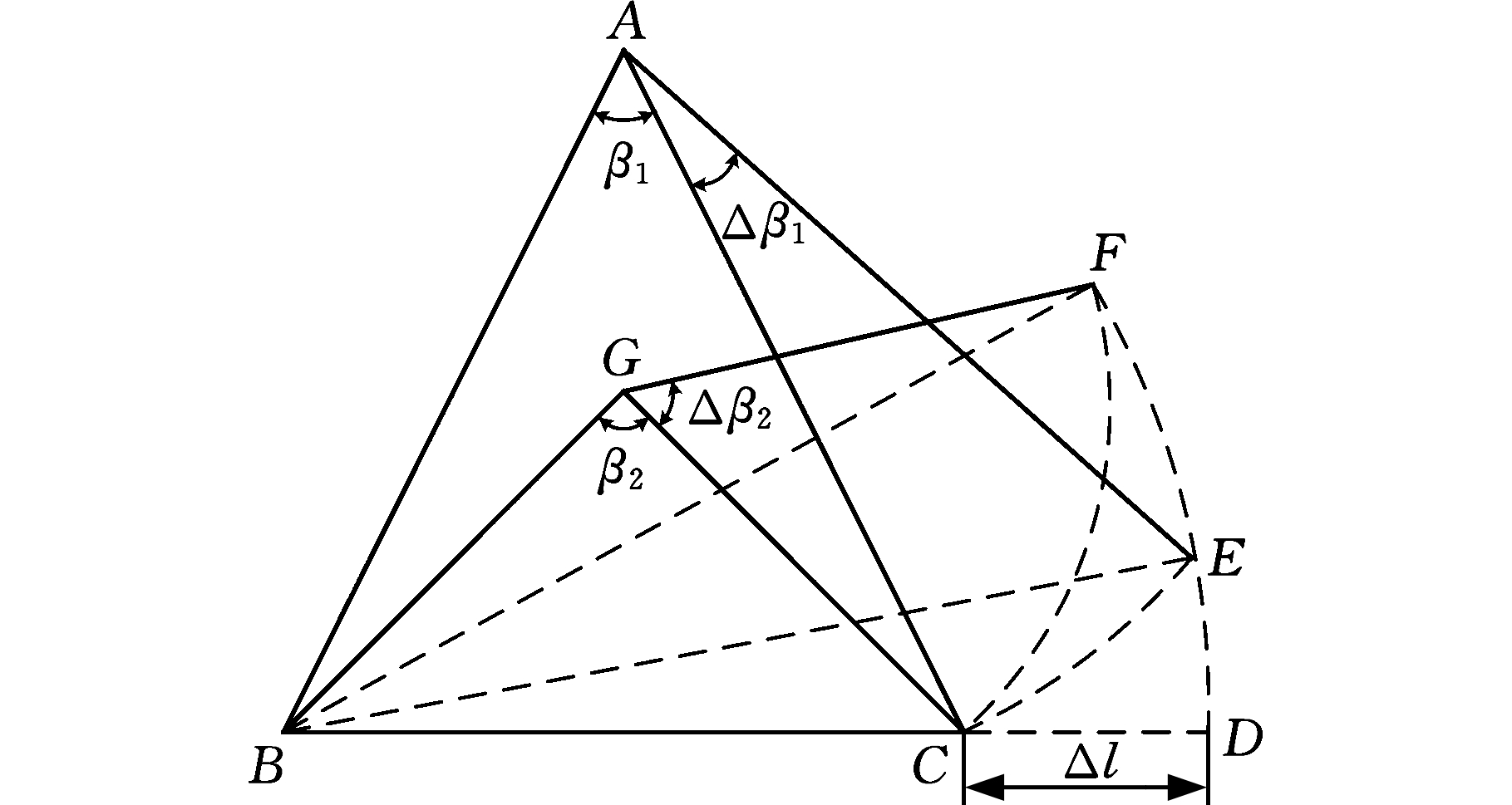
图5 支撑单元几何关系简化示意图
Fig.5 Schematic diagram of geometrical relationships
of simplified supporting elements
从图5中可以看出,∠EBD<∠FBD,且支架在扩张过程中,夹角增量通常小于90°,故∠EBD、∠FBD、Δβ1和Δβ2为锐角,则cosΔβ1-cosΔβ2>0,即Δβ1<Δβ2。所以,对于血管支架,当周向产生相同位移增量时,较小支撑单元夹角的增量较大。同时由于小支撑单元的原始夹角β2大于大支撑单元的夹角β1,最终导致支架扩张后小支撑单元夹角较大,因此,采用不等高支撑环的支架在扩张至相同直径后其径向支撑强度更大。
1.2 桥筋结构设计
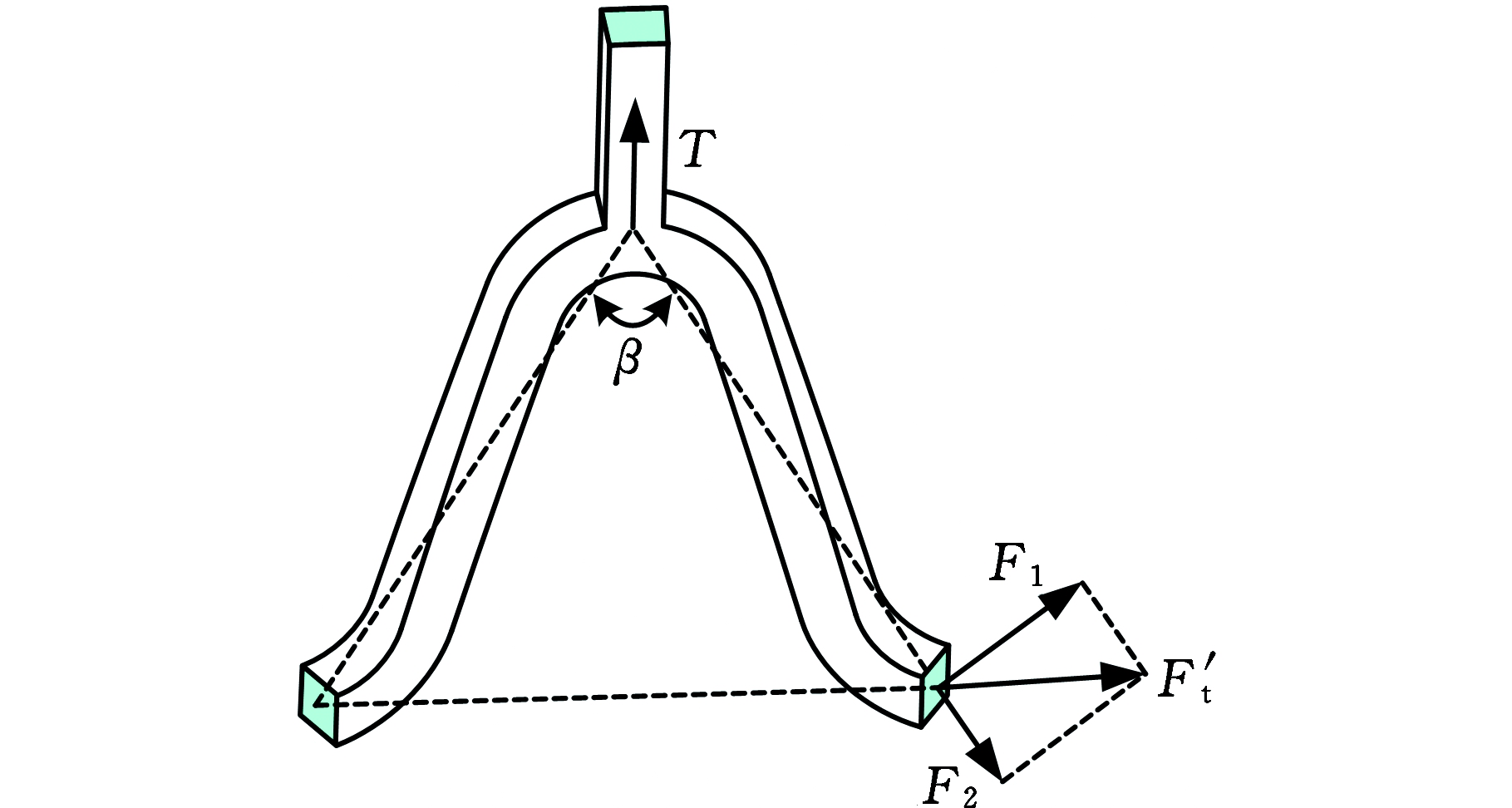
虽然桥筋的主要作用是将相邻两支撑环连接在一起,但是其结构形式对轴向短缩率也有一定影响。其原因是支架在扩张过程中,支架受到球囊压力p的作用,使得支撑单元受到周向力Ft(图6a、图6b)作用。Ft与p的关系可表达为
(7)
式中,Ft为支撑单元两端截面受到的周向力;p为球囊对支撑单元表面施加的内压力;α为支撑单元弧度;S为在α范围内支撑单元内表面面积。

(a)支撑环三维图
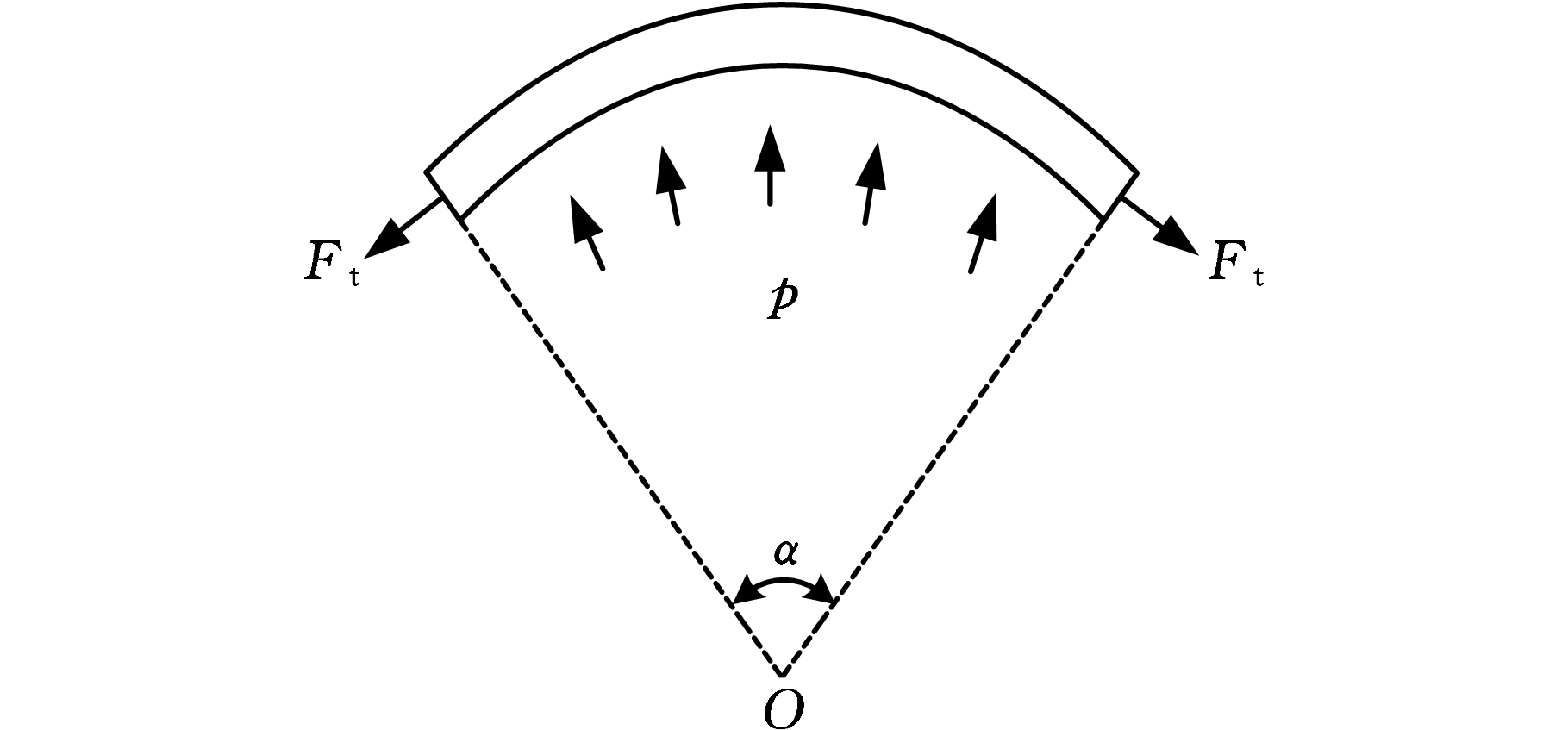
(b)支撑单元轴向视图
(c)支撑单元正向视图
图6 支撑环在球囊扩张作用下的受力示意图
Fig.6 Schematic diagram of supporting ring under the
action of the balloon expansion
为获得支撑单元内压力p与桥筋受到的拉伸力的关系,将支撑单元简化为平面等腰三角形,如图6c所示,则F′t=Ftcos(α/2),其中,F′t为简化后模型的周向拉伸力,可分解为F1和F2。从图6c中可以看出,F1为支架扩张的主要分力,F2使得支撑单元沿轴向运动,进而导致支撑单元的高度减小。因此,支撑环在扩张过程中,由于支撑单元高度的减小而发生轴向短缩。支撑环在变形过程中会对桥筋产生轴向拉力T,如图6c所示,T可表示为
(8)
式中,β为支撑单元夹角。
若桥筋在T的作用下伸长则可弥补支撑单元发生的短缩。然而,目前可降解聚合物支架的桥筋主要是直杆式结构,它在拉伸力T的作用下几乎不产生变形,因此,可通过设计合适的桥筋结构来减小支架的轴向短缩率。众所周知,相对直杆式结构,弯曲结构在拉伸力的作用下更容易变形,因此,本文设计了具有弯曲结构的桥筋。同时,考虑到目前对血管支架的加工主要采用激光雕刻的方法,而聚合物支架在加工过程中热影响区较大,因此桥筋的曲率不宜过大。
1.3 血管支架结构设计
可降解聚合物血管支架的典型结构如图7所示(如BVS)。该支架以具有类似正弦结构的等高支撑单元作为支撑环,直杆式结构作为桥筋,桥筋与支撑环的连接形式为开放式(同一支撑环上,相邻两桥筋构成的网孔内有一个以上的波峰或波谷)。该支架结构形式简单,易于加工,具有较好的弯曲刚度,但是这种支架结构的径向支撑强度较小,为获得较大的径向支撑强度,其壁厚通常比金属支架大得多[23]。

A.支撑环 B.直杆式桥筋 C.开放式结构
图7 典型的可降解聚合物血管支架结构二维图
Fig.7 Two-dimensional(2-D) sketch of typical
polymeric biodegradable vascular stent
考虑到径向支撑强度问题是制约可降解聚合物血管支架发展及广泛应用的主要问题,在结构设计时应着重提高该性能,同时兼顾径向回缩率、轴向短缩率和弯曲刚度。基于此,本文设计了以下三种支架结构:J型支架(J-type stent,JS),开放式C型支架(open C-type stent,OCS),密闭式C型支架(closed C-type stent,CCS)。
1.3.1 J型支架(JS)
JS支架二维图见图8,其结构特点是除两端的支撑环外,其他支撑环均采用不等高支撑环结构形式,以提高径向支撑强度;除两端的支撑环,其他支撑环呈同相排列,相位差为180°,使得桥筋空间较大,其弯曲段可具有较大尺寸,易于加工,且可以防止支架在紧缩过程中发生干涉;桥筋为J型结构(简称JS桥筋),与相邻的支撑环采用“波峰(波谷)-波峰(波谷)”连接,以改善支架的轴向短缩率;JS桥筋与支撑环采用开放式连接结构,以提高支架的弯曲刚度。其主要缺点是:为使JS桥筋具有较大空间,相邻两排支撑环的距离较大,与BVS相比,在相同长度下,支撑环数量较少,会导致径向支撑强度有所下降。

A.等高支撑环 B.直杆式桥筋 C.开放式结构 D.JS桥筋
E.不等高支撑环 F.小支撑单元 G.大支撑单元
图8 JS支架二维图
Fig.8 2-D sketch of JS stent
1.3.2 开放式C型支架(OCS)
为使支架结构在同一长度下具有更多的支撑环,设计了OCS(图9)。其结构特点是除两端的支撑环外,其他支撑环仍采用不等高支撑环结构形式,以提高径向支撑强度;除两端的支撑环外,其他支撑环呈异相排列,相位差为90°,使得相邻两排支撑环波峰(波谷)与波谷(波峰)间距较大,可以避免支架在弯曲过程中发生干涉;除两端的桥筋外,其他桥筋为C型结构(简称OCS桥筋),以改善支架的轴向短缩率;OCS桥筋的连接位置在支撑单元直线段的中间处,使得桥筋有较大的弯曲半径易于加工;OCS桥筋与支撑环采用开放式结构,以提高支架的弯曲刚度。相邻两排OCS桥筋开口方向相反,目的是防止扩张过程中发生转动。其主要缺点是:该支架在周向和轴向上均为非对称结构,在扩张过程中可能会出现膨胀不均匀现象。
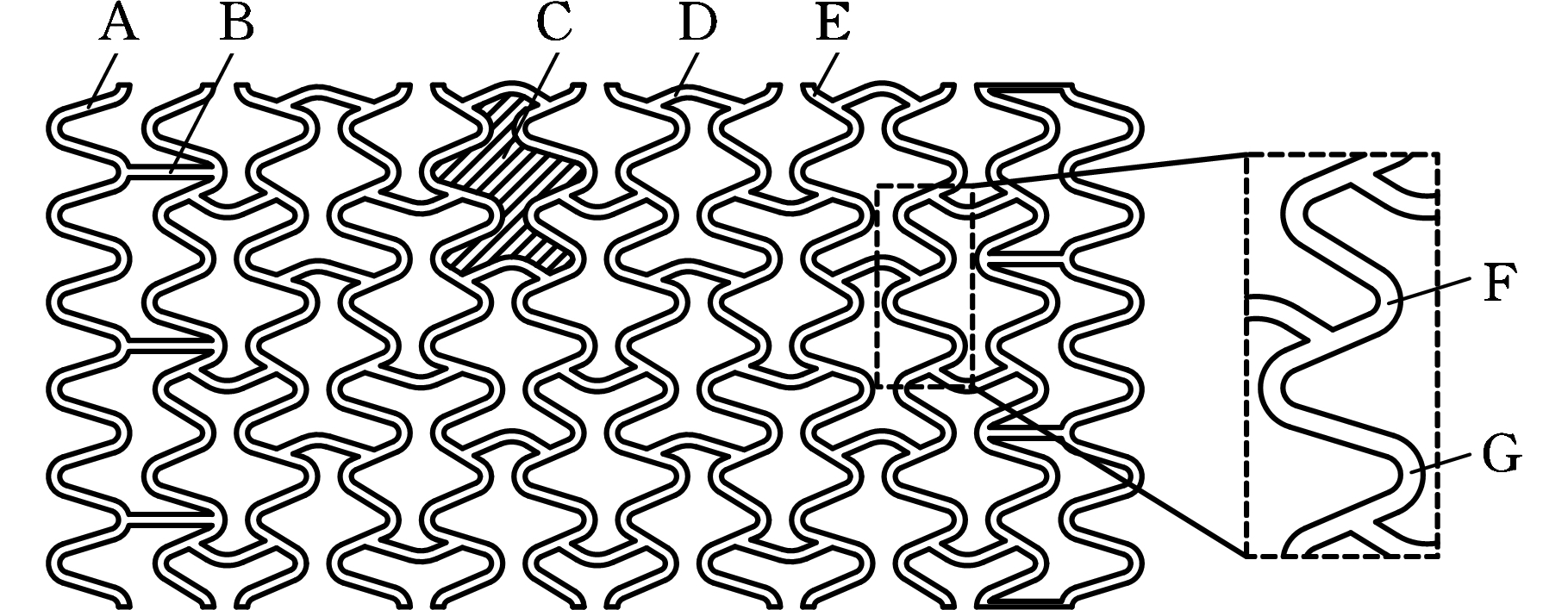
A.等高支撑环 B.直杆式桥筋 C.开放式结构 D.OCS桥筋
E.不等高支撑环 F.小支撑单元 G.大支撑单元
图9 OCS二维图
Fig.9 2-D sketch of OCS
1.3.3 密闭式C型支架(CCS)
为进一步提高OCS的径向支撑强度,设计了CCS(图10),该结构是在OCS基础上,将OCS桥筋与支撑环的连接形式由开放式改为密闭式(同一支撑环上,相邻两桥筋构成的网孔内均有一个波峰或波谷),同时为防止在支架扩张过程中桥筋与支撑环的连接位置出现过大的应力集中,相邻两排OCS桥筋的开口方向相同,将该桥筋结构命名为CCS桥筋。其主要缺点是:密闭式结构易减小支架的弯曲刚度。
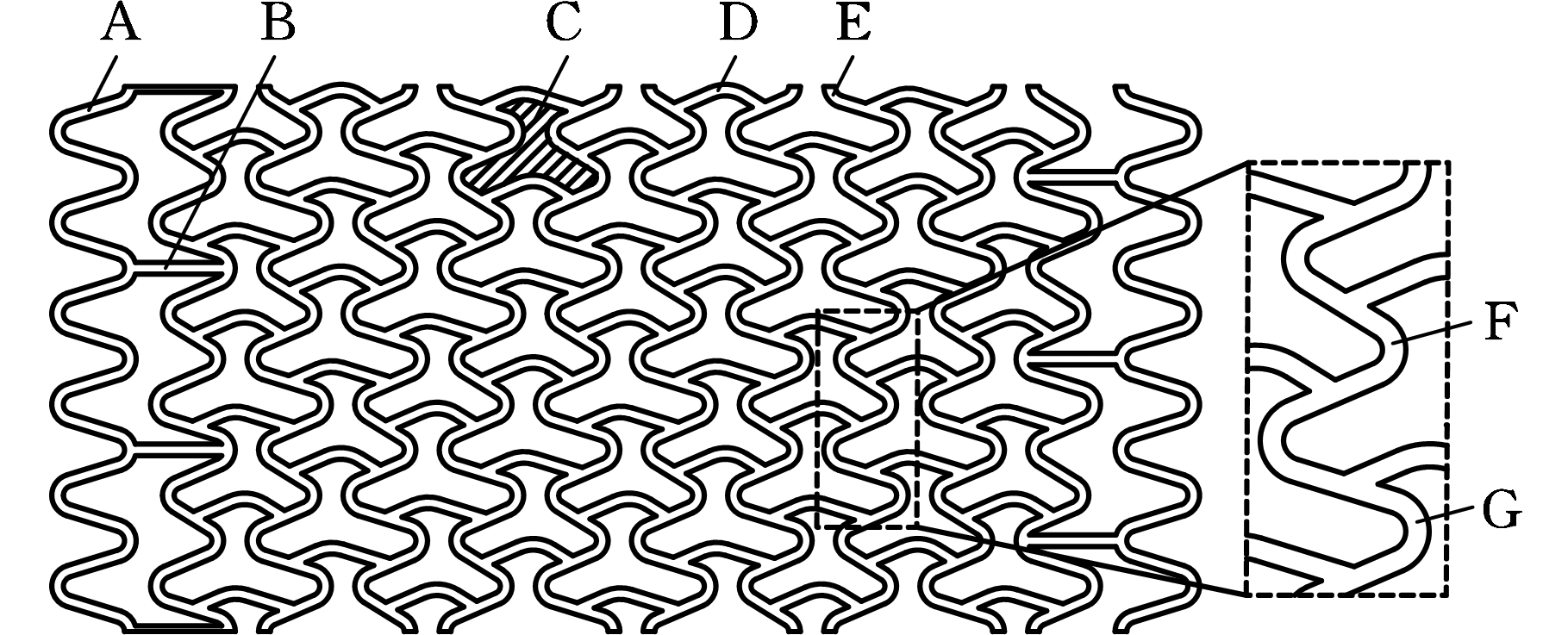
A.等高支撑环 B.直杆式桥筋 C.密闭式结构 D.CCS桥筋
E.不等高支撑环 F.小支撑单元 G.大支撑单元
图10 CCS二维图
Fig.10 2-D sketch of CCS
2 可降解聚合物血管支架力学性能有限元分析
为了分析所设计支架的合理性以及支架结构对径向支撑强度、径向回缩率、轴向短缩率和弯曲刚度的影响规律,采用ANSYS17.0软件包对所设计的三种支架的性能进行有限元分析计算,并以BVS作为对比。为使不同支架具有可比性,所设计的支架与BVS具有相同的外径(2.40 mm)、筋宽(0.15 mm)和筋厚(0.15 mm),支撑环周向具有相同的支撑单元数量。所设计支架的不等高支撑环的大支撑单元的高度与BVS支撑单元高度相同。此外,JS、OCS、CCS和BVS四种支架的长度分别为16.1 mm、15.5 mm、15.7 mm和16.1 mm。
径向支撑强度可通过对扩张后的支架进行平面压缩分析获得,根据此分析模型中的支架扩张阶段可以得到支架的径向回缩率和轴向短缩率。因扩张阶段先于压缩阶段,因此首先分析支架的径向回缩率和轴向短缩率。弯曲刚度可通过对支架两端施加弯矩获得。
2.1 有限元分析模型
2.1.1 支架扩张、平面压缩
以JS、OCS、CCS和BVS四种支架为研究对象,其扩张、平面压缩示意图见图11,包括血管支架、球囊、上压板和下压板。其中,支架采用8节点solid185实体单元沿厚度方向划分三层网格。球囊和上下压板均选用具有4节点壳单元shell181。JS、OCS、CCS和BVS单元数分别为20 520、20 988、26 820和21 834;球囊单元数为6 552,上下压板单元数为10 736。有限元三维模型(以BVS为例)如图12所示。
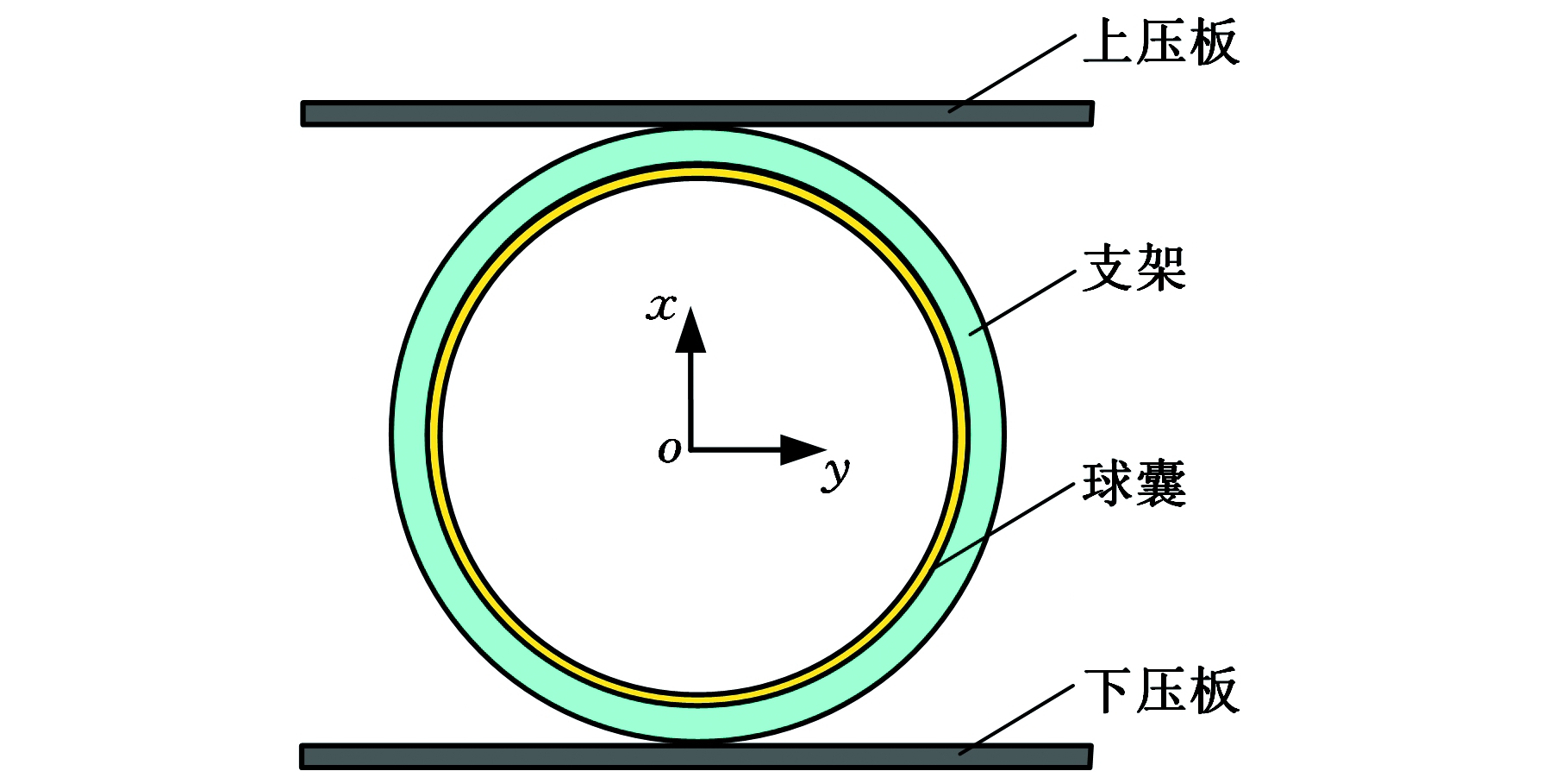
图11 支架扩张、平面压缩原理示意图
Fig.11 Schematic diagram of stent expansion and
planar compression
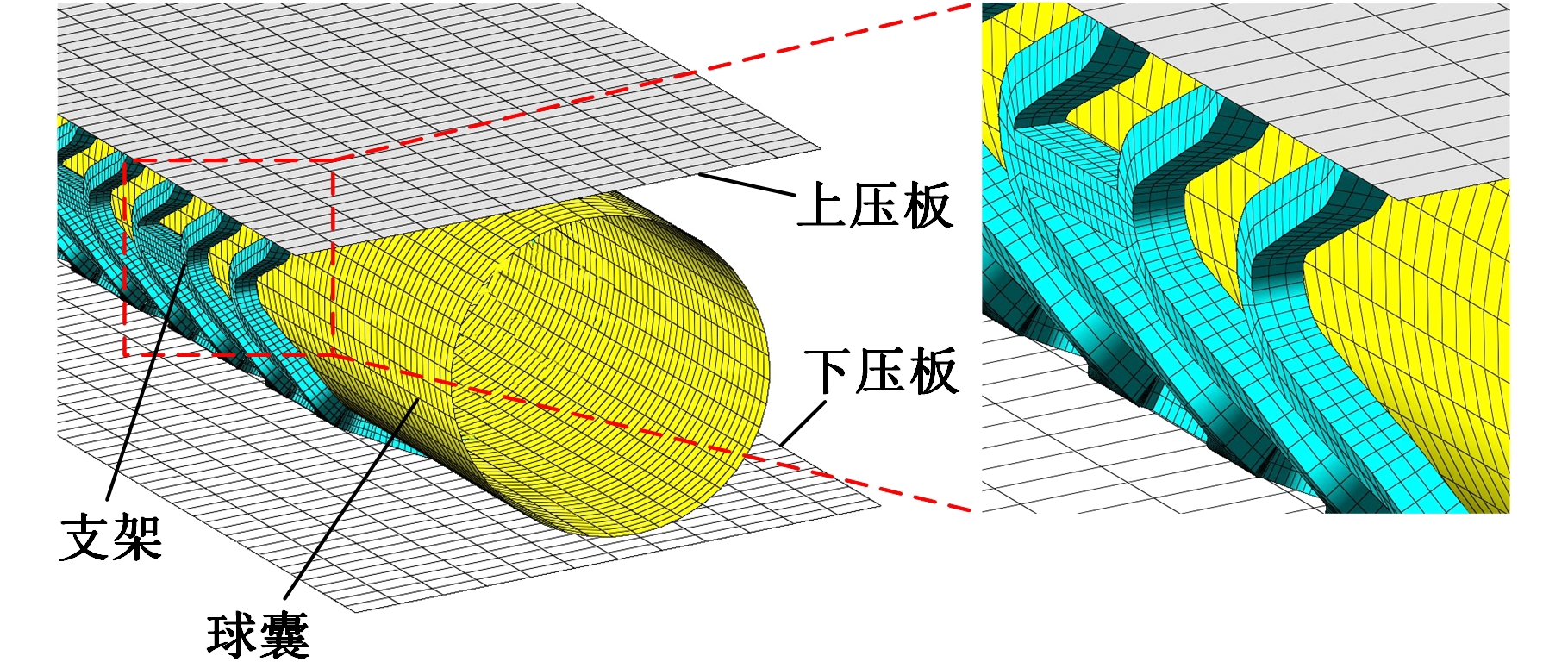
图12 支架扩张、平面压缩有限元三维模型
Fig.12 Three-dimensional(3-D) finite element model
of stent expansion and planar compression
2.1.2 弯曲
以JS、OCS、CCS和BVS为研究对象,图13所示为弯曲有限元三维模型(以BVS为例)。支架仍选用具有8节点的solid185实体单元,沿厚度方向划分三层网格。为了对支架均匀地施加弯矩,在支架两端的轴线位置分别建立两个刚性控制点A、B,并用mass21单元对其进行网格划分。

图13 弯曲有限元三维模型
Fig.13 3-D finite element model of the bending
2.2 材料特性
血管支架材料为聚乳酸(Ingeo 4032D,NatureWorks LLC,美国),其应力σ-应变ε曲线通过对加工的狗骨头试样进行拉伸试验获得,如图14所示。等效成双线性各向同性材料模型,弹性模量为3 546 MPa,屈服强度为51.5 MPa,泊松比为0.3。在支架扩张、平面压缩有限元模型中,球囊等效为两参数超弹性橡胶材料[25],其中C10 =1.068 8 MPa,C01=0.710 918 MPa;上下压板等效为刚性平面。
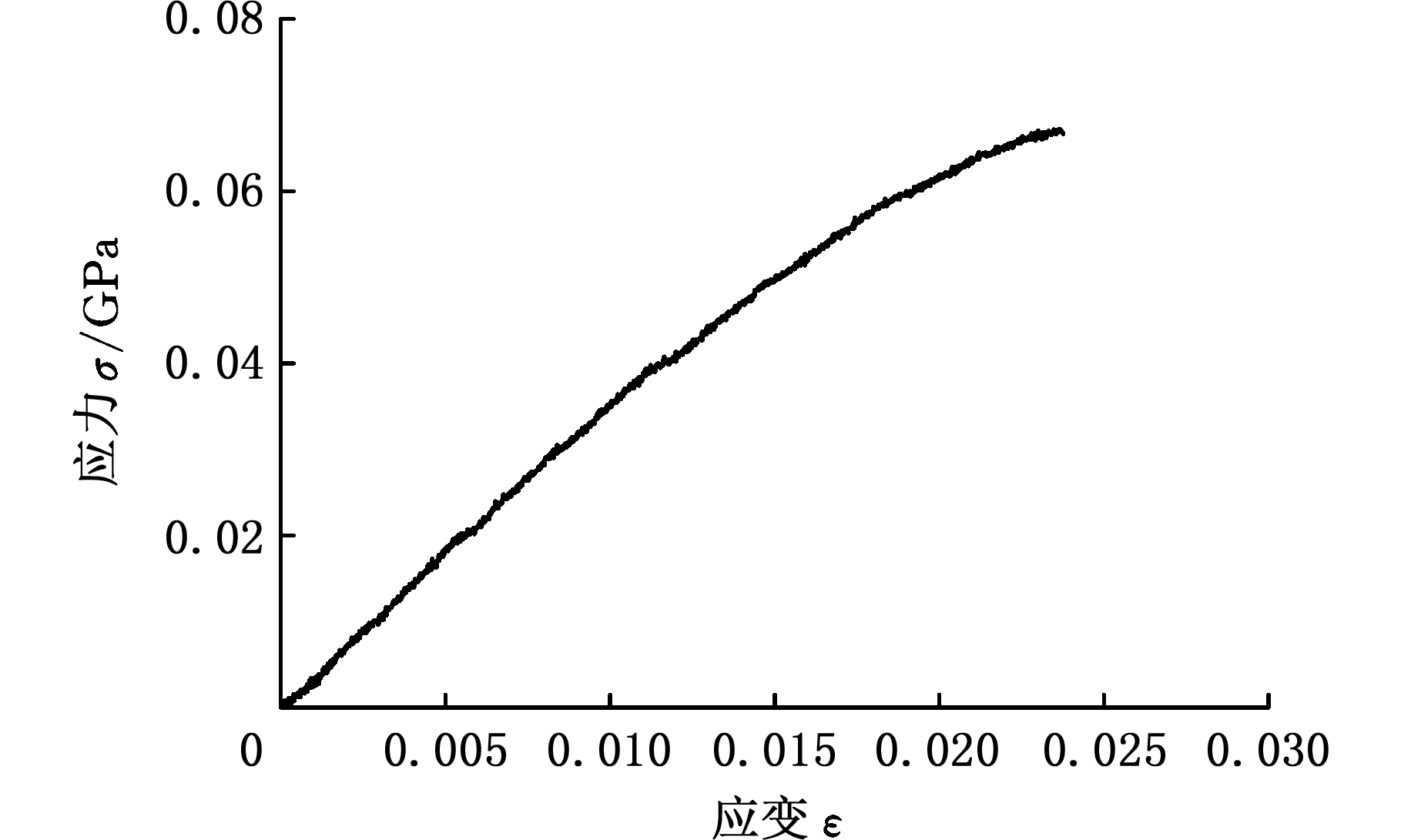
图14 聚乳酸应力-应变曲线
Fig.14 Stress-strain curve of the polylactic acid
2.3 载荷及边界条件
2.3.1 支架扩张、平面压缩分析
考虑到是在同一条件基础上对支架性能进行比较,为减少计算量,省略支架紧缩至球囊的过程,并采用位移载荷对球囊进行扩张[26-27]。考虑球囊与支架内表面、支架外表面与上下压板之间的接触,为模拟支架在球囊作用下扩张、球囊卸载后支架的变形和上下压板对支架压缩的全过程,分三步施加载荷:第一载荷步——球囊扩张,对球囊施加径向位移载荷x=0.3 mm,使球囊产生径向变形,并在接触作用下将血管支架撑开;对上下压板施加除x方向位移外所有约束。第二载荷步——球囊卸载,对球囊施加径向位移载荷x=0,使支架自由回缩。第三载荷步——平面压缩,对上平板施加方向竖直向下、大小随时间线性变化的均布力载荷;约束下平板所有自由度,并杀死球囊与支架内表面的接触单元。
2.3.2 弯曲分析
将两个刚性控制点A和B分别与支架两端部节点耦合。对两控制点施加弯矩M,为防止支架模型在空间内平动,约束控制点x、y方向的刚体位移,同时,防止支架绕y轴和z轴转动,约束控制点在相应方向上的转动,如图13所示。其中,φ为施加弯矩后控制点转角。
2.4 血管支架力学性能
(1)径向回缩率η。径向回缩率指从球囊扩张到球囊卸载后支架的直径尺寸变化,通常可表示为[28]
(9)
式中,Dde为球囊卸载后支架的外径;Din为球囊扩张后支架的外径。
(2)轴向短缩率μ。轴向短缩率指支架从非展开状态至扩张到标称直径后长度的变化比,其计算公式为[29]
(10)
式中,L为支架非展开状态长度;Lde为球囊卸载后支架的长度。
(3)径向支撑强度。径向支撑强度指支架抵抗血管壁收缩的能力,采用支架压缩过程的压缩载荷pload-位移s曲线来表征。为使不同长度支架的径向支撑强度具有可比性,力载荷要归一化,其公式为[30]
(11)
式中,F为均布力载荷总值。
(4)弯曲刚度k。弯曲刚度是指支架的轴向弯曲能力,可表示为[31]
(12)
式中,M为作用于支架端部的弯矩;2φ/L为支架单位长度上的转角。
3 分析结果与讨论
3.1 支架扩张有限元分析
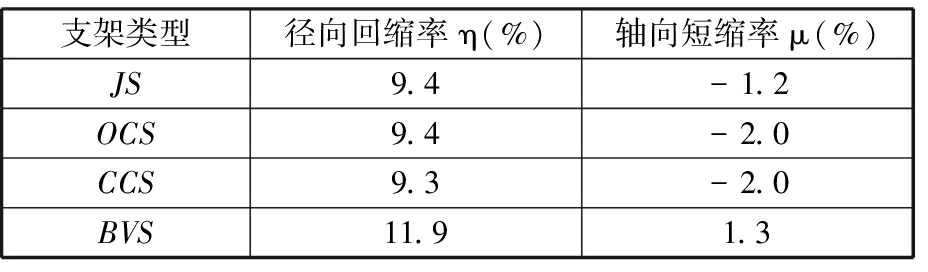
根据支架扩张分析结果,可以得到四种支架的径向回缩率和轴向短缩率,如表1所示。
表1 不同支架的径向回缩率和轴向短缩率
Tab.1 Radial recoil and axial foreshortening of
different stents
支架类型径向回缩率η(%)轴向短缩率μ(%)JS9.4-1.2OCS9.4-2.0CCS9.3-2.0BVS11.91.3
3.1.1 径向回缩率
从表1中可以看出,JS、OCS和CCS的径向回缩率几乎相等,相比BVS的径向回缩率减小了约21%。支架发生径向回缩的原因是支架被扩张后仍存在一定的弹性形变。所设计的三种支架的径向回缩率小于BVS的径向回缩率是因为这三种支架采用了不等高支撑环。根据前文可知,当周向产生相同位移增量时,不等高支撑环的小支撑单元夹角增量较大,即变形较大,则所设计支架的不等高支撑环发生更多的塑性形变,弹性变形区减小,因此径向回缩率减小。
此外,支架扩张后,弹性恢复力Fe可分解为沿周向的分力Fe1和沿轴向的分力Fe2,如图15所示。周向力Fe1是支架直径变小的主要因素,可表示为
Fe1=Fecosθ
(13)
Fe1随θ增大而减小,θ近似等于支撑单元夹角β(0°≤β≤180°)的一半,因此,在相同弹性恢复力情况下,支撑单元夹角越大,周向分力Fe1越小。根据前文可知,支架扩张至同一直径后,不等高支撑环中小支撑单元的夹角较大。且因其发生更多的塑性变形,则弹性恢复力较小,那么根据式(13)可知,最终作用于支撑单元的周向分力Fe1更小。因此,所设计的支架具有较小的径向回缩率。
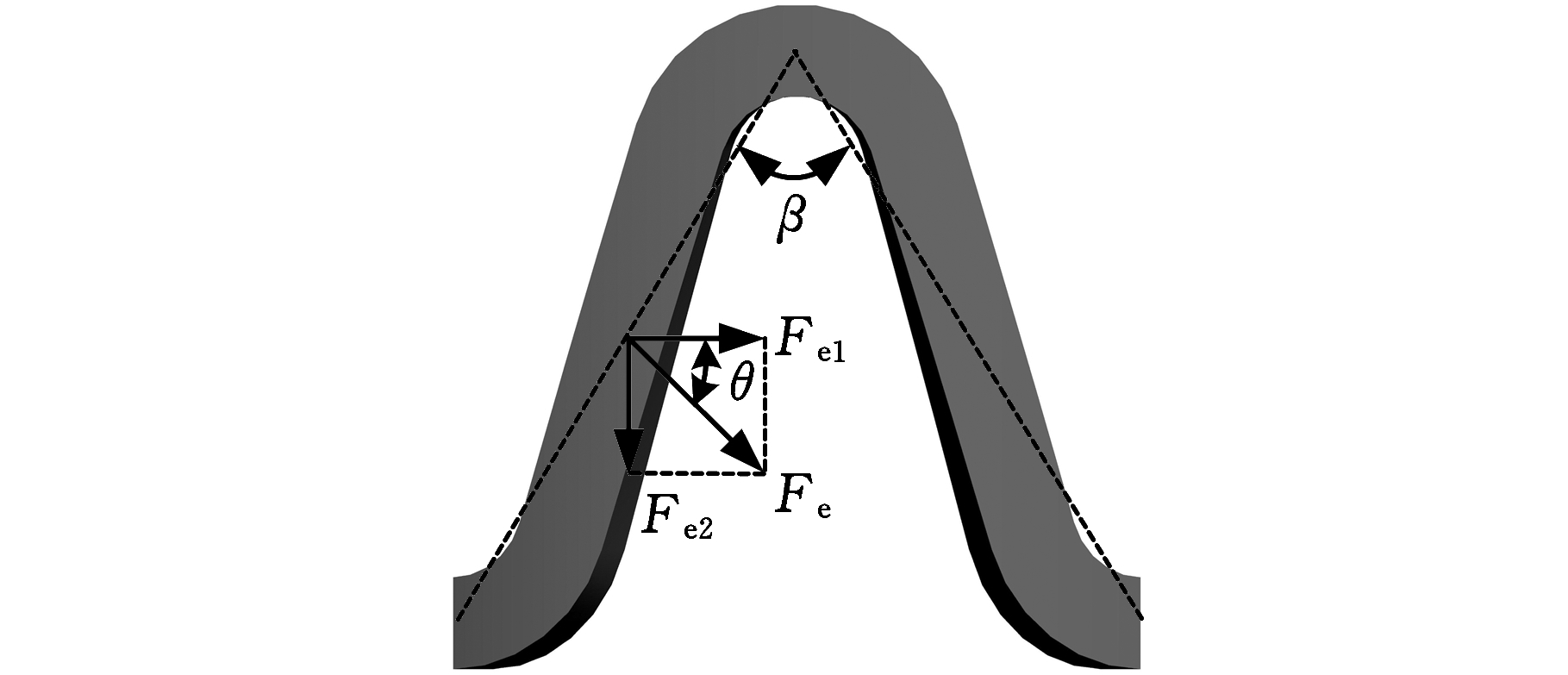
图15 支撑单元在弹性恢复力作用下的受力示意图
Fig.15 Schematic diagram of supporting ring suffered
from the elastic restoring force
图16为球囊扩张后支架的局部变形图,可以看出,所设计的三种支架的小支撑单元夹角(θ1≈100°,θ2≈97°,θ3≈104°)均明显大于BVS支撑单元的夹角(θ4≈78°),验证了上述观点。

(a)JS (b)OCS

(c)CCS (d)BVS
图16 不同类型支架扩张后的局部变形图
Fig.16 Local deformations of the different type
stents after expansion
3.1.2 轴向短缩率
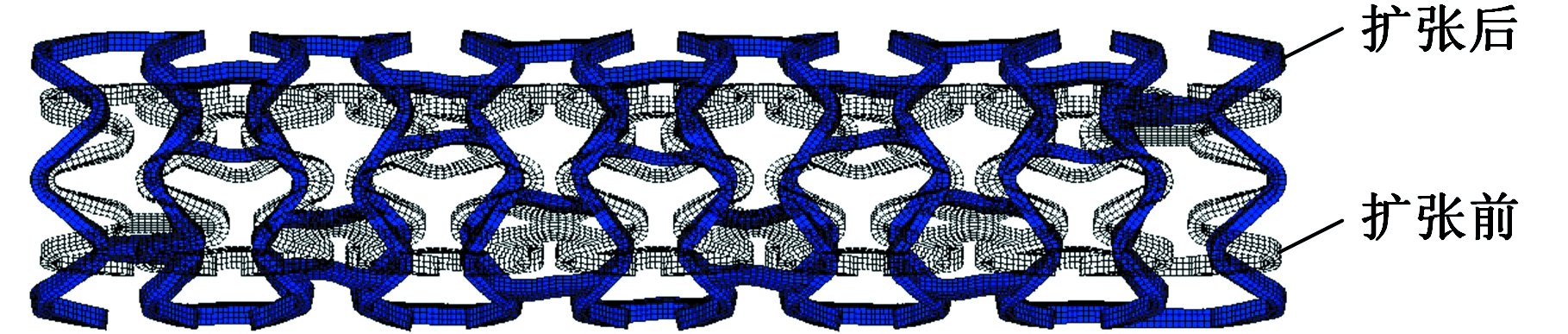
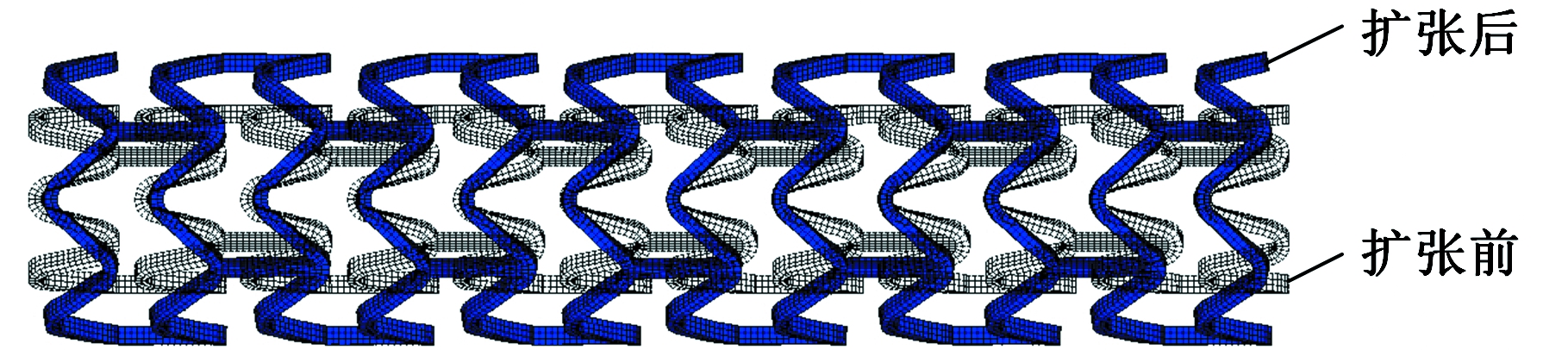
从表1中可以看出,BVS的轴向短缩率最大,所设计的三种支架短缩率为负值,说明它们非但没有缩短反而有所伸长。其中,CCS和OCS的伸长量相等,且大于JS的伸长量。所设计的三种支架的轴向短缩率为负值是因为在支架扩张过程中,支撑环高度减小,导致桥筋在轴向力T(图6c)的作用下不同程度地伸长,且伸长量大于支撑环的缩短量,故轴向短缩率为负值。而BVS的桥筋为直杆式结构,在扩张过程中长度几乎不变,故支架缩短,且轴向短缩率较大。CCS和OCS的伸长量大于JS 支架的伸长量是因为CCS桥筋和OCS桥筋的连接位置在支撑单元直线段的中间处,在扩张过程中,支撑单元在周向力Ft作用下逐渐被“拉直”,OCS桥筋和CCS桥筋在连接位置受到弯矩Mt作用(图17),使其相对JS桥筋更容易张开而伸长,故OCS和CCS的伸长量要大于JS的伸长量。四种支架扩张前后的变化如图18所示,可以看出所设计的三种支架在轴向均有不同程度的伸长,而BVS发生了明显的短缩。
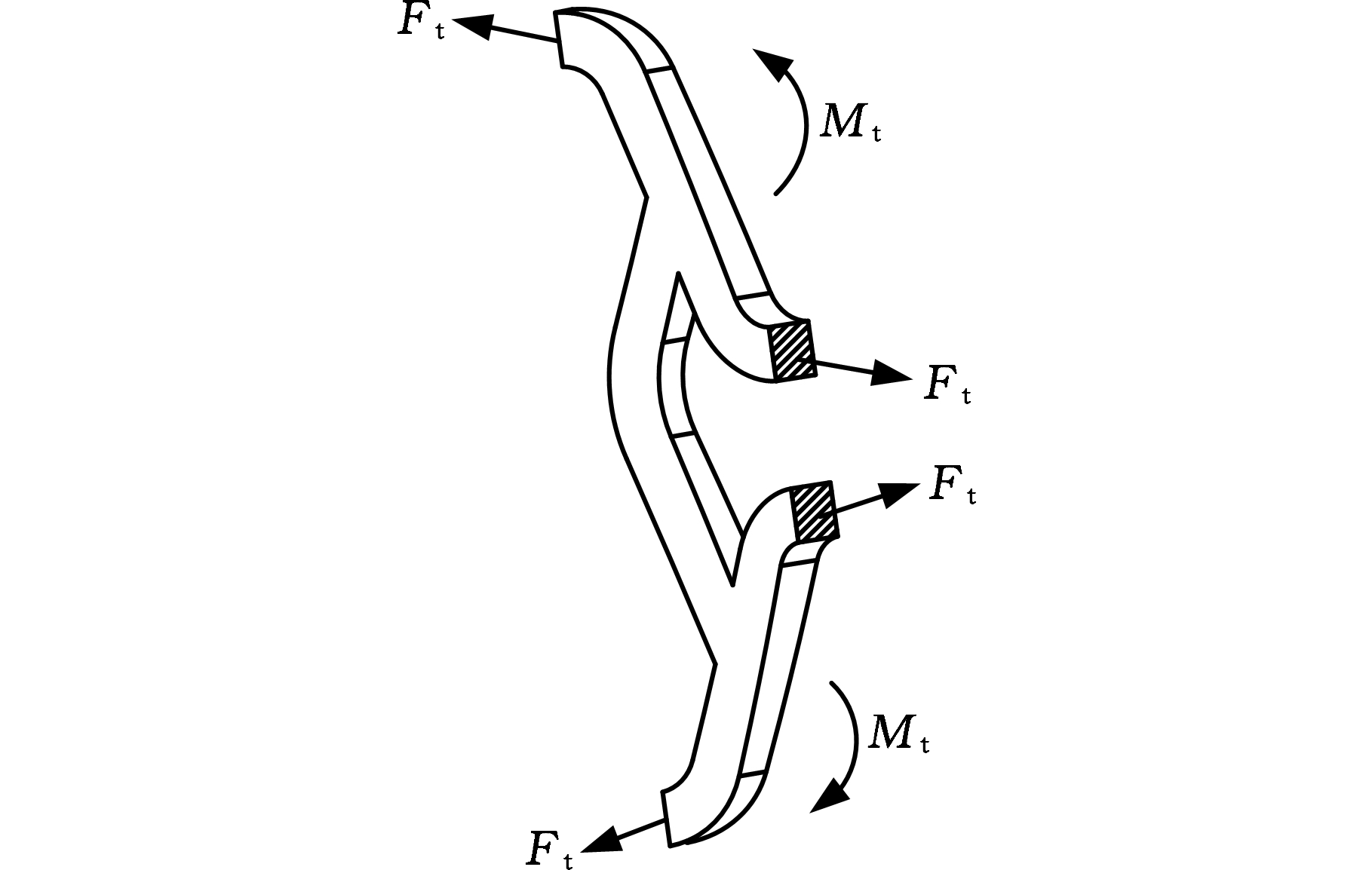
图17 支架扩张过程中OCS桥筋或CCS桥筋
受力示意图
Fig.17 Schematic diagram of OCS bridge or CCS
bridge during stent expansion

(a)JS
(b)OCS

(c)CCS
(d)BVS
图18 不同类型支架扩张前后变形图
Fig.18 Deformations of different type stents before
and after expansion
3.2 平面压缩有限元分析
根据平面压缩分析结果可以得到四种支架的压缩载荷-位移曲线,如图19所示。将支架压缩至扩张后支架直径的50%时所需的压缩载荷作为支架的径向支撑强度,则JS、OCS、CCS和BVS的径向支撑强度分别为79.9 N/m、94.4 N/m、99.9 N/m、70.2 N/m。
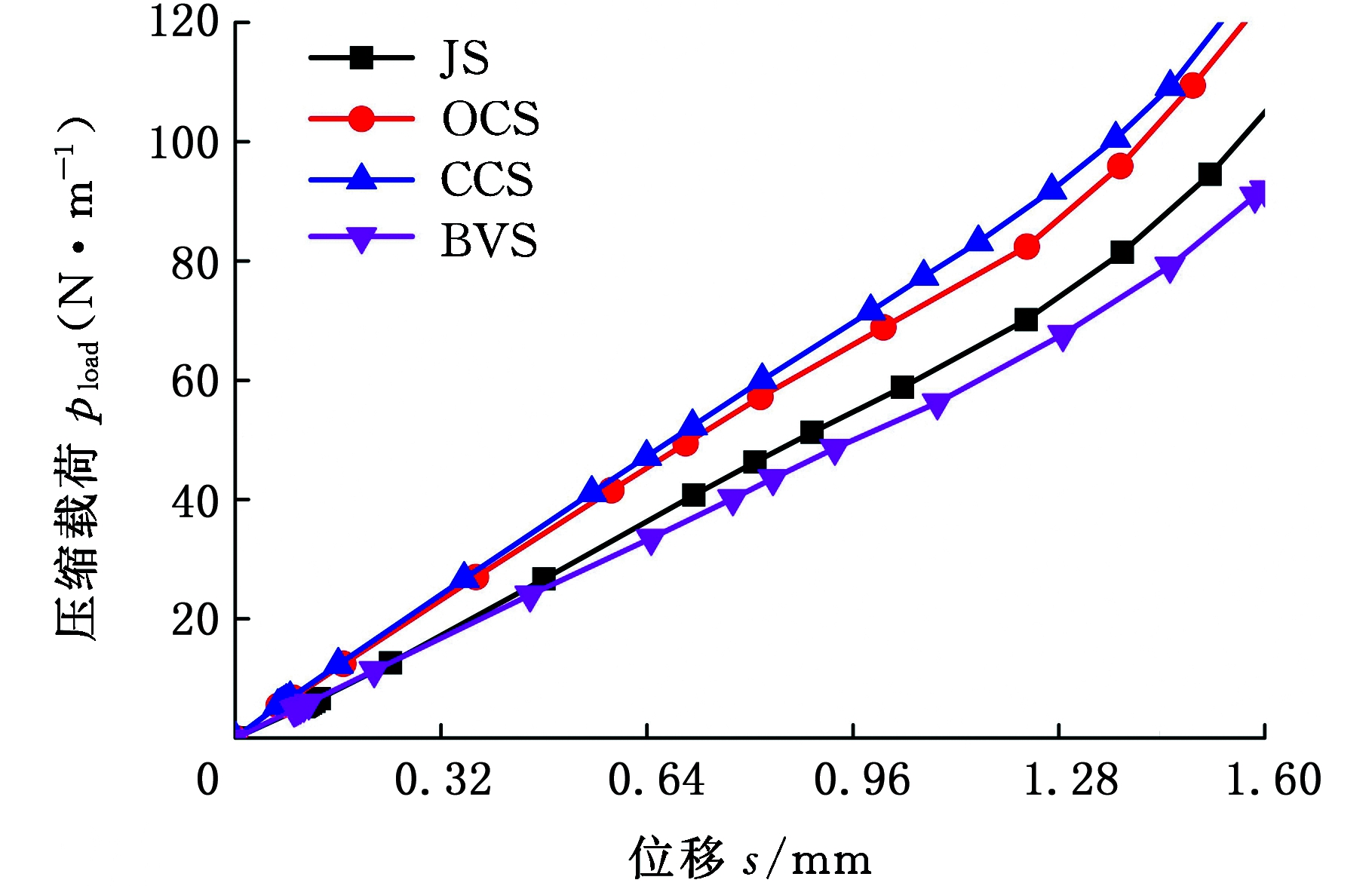
图19 不同类型支架压缩载荷-位移关系曲线
Fig.19 Compressive load-displacement curves of
different type stents
可以看出,JS、OCS和CCS的径向支撑强度相对BVS的径向支撑强度分别提高了14%、34%和42%。其原因是所设计的三种支架均采用了不等高支撑环,因此其径向支撑强度相对BVS均有所提高。在支架长度近似相同的情况下,OCS和CCS的支撑环数量多于JS的支撑环数量,故二者径向支撑强度大于JS的径向支撑强度。由于CCS相对OCS在结构形式上具有更大的刚度,且桥筋数量的增加也在一定程度上起到了抵抗外力变形的作用,故CCS径向支撑强度要大于OCS的径向支撑强度。
3.3 弯曲有限元分析
根据弯曲有限元分析结果可以获得弯矩M与支架单位长度上的转角κ关系,如图20所示。根据弯曲刚度表达式(式(11))可以看出,弯曲刚度可以看作是弯矩-转角曲线斜率的倒数。取变形初期部分的曲线(0<M<0.05 N·mm,即弹性变形阶段)并测量其斜率,得到JS、OCS和BVS的弯曲刚度几乎相同,为3.2 N·mm2,CCS弯曲刚度为11.9 N·mm2。

图20 不同类型支架弯矩与转角的关系曲线
Fig.20 Bending moment-rotate angle curves of
different type stents
根据不同支架的弯曲刚度可以看出,JS、OCS和BVS的弯曲刚度相当,且相对CCS的弯曲刚度减小了约73%。其原因是,支架变形初期弯矩较小,桥筋几乎不发生变形,弯曲刚度主要受桥筋与支撑环的连接方式影响。密闭式结构支架的每一支撑单元均有桥筋相连,使其在弯矩作用下不易发生弯曲,故CCS弯曲刚度高于其他三种支架的弯曲刚度。此外,根据弯矩与转角关系曲线可以看出,随着弯矩逐渐增大,OCS和JS的弯曲刚度略大于BVS的弯曲刚度,其原因是随着弯矩的增大,桥筋逐渐发生变形,而OCS桥筋和JS桥筋相对BVS的直杆式桥筋更容易弯曲,因此,OCS和JS的弯曲刚度大于BVS的弯曲刚度,但是由于支架在弯曲过程中,其变形主要是支撑环沿x方向转动(图13),桥筋的形变量较小,因此,桥筋对弯曲柔顺性的影响不明显。
通过以上分析可以看出,所设计的三种支架的径向支撑强度均大于BVS的径向支撑强度,其中CCS最大,OCS次之,二者较为接近,JS的径向支撑强度虽大于BVS的径向支撑强度,但优势不明显。可见,对径向支撑强度影响的主要因素是不等高支撑环的结构形式,密闭式结构在一定程度上也能提高径向支撑强度,但效果不显著。JS虽然采用了不等高支撑环,但由于它在相同支架长度下,支撑环数量较少,所以径向支撑强度提高得不明显。影响径向回缩率的主要因素是支撑环的结构形式,不等高支撑环可显著改善径向回缩率。影响轴向短缩率的主要因素是桥筋的结构形式和桥筋的连接位置,JS桥筋、OCS桥筋和CCS桥筋均可有效改善支架的轴向短缩率,其中OCS桥筋和CCS桥筋的连接位置位于支撑环直线段的中间处,使得桥筋更容易变形,从而改善支架的轴向短缩率。影响弯曲刚度的主要因素是桥筋与支撑环的连接形式,采用开放式连接的支架弯曲刚度更高,桥筋结构形式虽有利于提高弯曲刚度,但由于在弯曲过程桥筋变形较小,所以影响很小。
综合分析所设计的三种支架的径向支撑强度、径向回缩率、轴向短缩率和弯曲刚度,OCS和CCS具有较高的径向支撑强度,且径向回缩率和轴向短缩率也均小于BVS的径向回缩率和轴向短缩率,虽然CCS的弯曲刚度小于BVS的弯曲刚度,但通常聚合物支架的弯曲刚度要远远大于金属支架的弯曲刚度,因此可降解聚合物血管支架采用这两种支架结构其综合性能更好。
4 结论
(1)针对可降解聚合物血管支架径向支撑强度较弱的问题设计了JS、OCS和CCS三种支架。通过有限元方法综合分析了三种支架和BVS的径向支撑强度、径向回缩率、轴向短缩率和弯曲刚度,并研究了支架结构对上述性能的影响规律。
(2)提出了采用不等高支撑环以利于增大扩张后支撑单元夹角进而提高径向支撑强度的设计方法,根据该方法设计的三种支架的径向支撑强度与BVS支架的径向支撑强度相比均有不同程度的提高,验证了设计方法的正确性;提出采用具有弯曲结构桥筋可减小支架轴向短缩率的观点,所设计的三种支架的桥筋均为弯曲结构,通过有限元分析,三种支架在扩张后均未发生短缩,验证了桥筋设计方法的正确性。
(3)通过对支架进行结构设计可有效改善支架的径向支撑强度。JS、OCS和CCS的径向支撑强度相对BVS的径向支撑强度分别提高了14%、34%和42%。影响径向支撑强度的主要因素是支撑环的结构形式,不等高支撑环可有效改善径向支撑强度,其原因是不等高支撑环的小支撑单元在扩张后具有较大的支撑单元夹角,增强了支架抵抗径向变形的能力。
(4)所设计的三种支架的径向回缩率相当,且相对BVS的径向回缩率减小了约21%。影响径向回缩率的主要因素是支撑环的结构形式,采用不等高支撑环可明显减小径向回缩率,其主要原因是不等高支撑环的小支撑单元在扩张后发生更多的塑性变形,降低了支架的弹性回缩。
(5)JS、OCS和CCS的轴向短缩率分别为-1.2%、-2.0%和-2.0%,说明这三种支架在轴向非但没有短缩,反而略有伸长。影响支架轴向短缩率的主要因素是桥筋的结构形式和桥筋的连接位置,采用具有弯曲结构的桥筋且桥筋的连接位置在支撑单元直线段的中间处可有效减小支架的轴向短缩率。其原因是支架在扩张时,具有弯曲结构的桥筋在轴向力作用下伸长,从而弥补了支撑环的短缩;桥筋的连接位置位于支撑单元直线段的中间处使桥筋在弯矩作用更容易“伸直”。
(6)JS、OCS与BVS的弯曲刚度相当,其弯曲刚度为3.2 N·mm2,CCS的弯曲刚度为11.9 N·mm2。影响弯曲刚度的主要因素是桥筋与支撑环的连接形式,相对密闭式连接,开放式连接的支架弯曲刚度更好,其原因是密闭式结构支架的每一支撑单元均有桥筋相连,使其在弯矩作用下不易发生弯曲。
[1] BRIE D, PENSON P, SERBAN M C, et al. Bioresorbable Scaffold—a Magic Bullet for the Treatment of Coronary Artery Disease[J]. International Journal of Cardiology, 2016, 215:47-59.
[2] BOLAND E L, SHINE R, KELLY N, et al. A Review of Material Degradation Modelling for the Analysis and Design of Bioabsorbable Stents[J]. Annals of Biomedical Engineering, 2015, 44(2):341-356.
[3] GOGAS B D. Bioresorbable Scaffolds for Percutaneous Coronary Interventions[J]. Global Cardiology Science and Practice, 2014, 2014(4):409-427.
[4] WIEBE J, NEF H M, HAMM C W. Current Status of Bioresorbable Scaffolds in the Treatment of Coronaryartery Disease[J]. Journal of the American College of Cardiology, 2014, 64(23):2541-2551.
[5] 郑利萍,贾莉芳,袁暾,等.新型可降解聚合物血管支架的体内血栓形成评价[J].生物医学工程学杂志, 2019, 36(2):1-6.
ZHENG Liping, JIA Lifang, YUAN Tun, et al. The in vivo Thrombosis Evaluation for the Biodegradable Polymer Stent[J]. Journal of Biomedical Engineering, 2019, 36(2):1-6.
[6] CAIAZZO G, KILIC I D, FABRIS E, et al. Absorb Bioresorbable Vascular Scaffold: What Have We Learned after 5 Years of Clinical Experience?[J]. International Journal of Cardiology, 2015, 201: 129-136.
[7] SOARES J S, MOORE J E. Biomechanical Challenges to Polymeric Biodegradable Stents[J]. Annals of Biomedical Engineering, 2016, 44(2):1-20.
[8] FOIN N, LEE R D, TORII R, et al. Impact of Stent Strut Design in Metallic Stents and Biodegradable Scaffolds [J]. International Journal of Cardiology, 2014, 177(3):800-808.
[9] HUI Y A, BULLUCK H, WONG P, et al. Bioresorbable Stents: Current and Upcoming Bioresorbable Technologies[J]. International Journal of Cardiology, 2017, 228:931-939.
[10] TENEKECIOGLU E, FAROOQ V, BOURANTAS C V, et al. Bioresorbable Scaffolds: a New Paradigm in Percutaneous Coronary Intervention[J]. BMC Cardiovascular Disorders, 2016, 16(1): 38.
[11] HOU Lida, LI Zhen, PAN Yu, et al. A Review on Biodegradable Materials for Cardiovascular Stent Application[J]. Frontiers of Materials Science, 2016, 10(3):238-259.
[12] LINDHOLM D, JAMES S. Bioresorbable Stents in PCI[J]. Current Cardiology Reports, 2016, 18(8):1-6.
[13] KOCKA V, TOUSEK P, WIDIMSKY P. Absorb Bioresorbable Stents for the Treatment of Coronary Artery Disease[J]. Expert Review of Medical Devices, 2015, 12(5):545-557.
[14] ALEXY R D, LEVI D S. Materials and Manufacturing Technologies Available for Production of a Pediatric Bioabsorbable Stent[J]. BioMed Research International, 2013, 18:137985.
[15] ANG H Y, HUANG Y Y, LIM S T, et al. Mechanical Behavior of Polymer-based vs. Metallic-based Bioresorbable Stents[J]. Journal of Thoracic Disease, 2017, S9:S923.
[16] 赵丹阳,刘韬,李红霞,等. 可降解聚合物血管支架结构优化设计[J].力学学报, 2017, 49(6):1409-1417.
ZHAO Danyang, LIU Tao, LI Hongxia, et al.Optimization Design of Degradable Polymer Vascular Stent Structure[J]. Chinese Journal of Theoretical and Applied Mechanics, 2017, 49(6):1409-1417.
[17] 李萍萍, 张若京. 具有周期结构的血管支架有限元分析[J]. 工程力学, 2012, 29(9):369-374.
LI Pingping, ZHANG Ruojing. Finite Element Analysis of Stent with Periodic Structure[J]. Engineering Mechanics, 2012, 29(9):369-374.
[18] WU W, PETRINI L, GASTALDI D, et al. Finite Element Shape Optimization for Biodegradable Magnesium Alloy Stents[J]. Annals of Biomedical Engineering, 2010, 38(9):2829-2840.
[19] HSIAO H M, CHIU Y H, LEE K H, et al. Computational Modeling of Effects of Intravascular Stent Design on Key Mechanical and Hemodynamic Behavior[J]. Computer-Aided Design, 2012, 44(8):757-765.
[20] AZAOUZI M, MAKRADI A, BELOUETTAR S. Numerical Investigations of the Structural Behavior of a Balloon Expandable Stent Design Using Finite Element Method[J]. Computational Materials Science, 2013, 72(9):54-61.
[21] MORI K, SAITO T. Effects of Stent Structure on Stent Flexibility Measurements[J]. Annals of Biomedical Engineering, 2005, 33(6):733.
[22] FENG Q, JIANG W, SUN K, et al. Mechanical Properties and in Vivo Performance of a Novel Sliding-lock Bioabsorbable Poly-dioxanone Stent[J]. Journal of Materials Science Materials in Medicine, 2011, 22(10):2319-2327.
[23] BOURANTAS C V, ZHANG Y J, FAROOQ V, et al. Bioresorbable Scaffolds: Current Evidence and Ongoing Clinical Trials[J]. Current Cardiology Reports, 2012, 14(5): 626-634.
[24] YANG J, HUANG N. Mechanical Formula for the Plastic Limit Pressure of Stent during Expansion[J]. Acta Mechanica Sinica, 2009, 25(6):795-801.
[25] LI H, LIU T, WANG M, et al. Design Optimization of Stent and Its Dilatation Balloon Using Kriging Surrogate Model[J]. Biomedical Engineering Online, 2017, 16(1):13.
[26] TAKASHIMA K, KITOU T, MORI K, et al. Simulation and Experimental Observation of Contact Conditions between Stents and Artery Models[J]. Medical Engineering & Physics, 2007, 29(3):326-335.
[27] LI Junlei, ZHENG Feng, QIU Xun, et al. Finite Element Analyses for Optimization Design of Biodegradable Magnesium Alloy Stent[J]. Materials Science & Engineering C, 2014, 42:705-714.
[28] ASTM International. F2079—09(2017) Standard Test Method for Measuring Intrinsic Elastic Recoil of Balloon-Expandable Stents[S]. West Conshohocken, PA: ASTM International Press, 2017: 1-3.
[29] ASTM International. F2081—06(2017) Standard Guide for Characterization and Presentation of the Dimensional Attributes of Vascular Stents[S]. West Conshohocken, PA: ASTM International Press, 2017:1-3.
[30] ASTM International. F3067—14 Guide for Radial Loading of Balloon Expandable and Self Expanding Vascular Stents[S]. West Conshohocken, PA: ASTM International Press, 2014:1-3.
[31] 李红霞. 冠脉支架的力学行为研究及其优化设计[D].大连:大连理工大学,2014.
LI Hongxia. Mechanical Behavior Research and Design Optimization of Coronary Stent[D]. Dalian: Dalian University of Technology, 2014.
